Неинвазивные способы визуализации выявляют рак на молекулярном уровне
|
By LabMedica International staff writers Posted on 20 Sep 2019 |
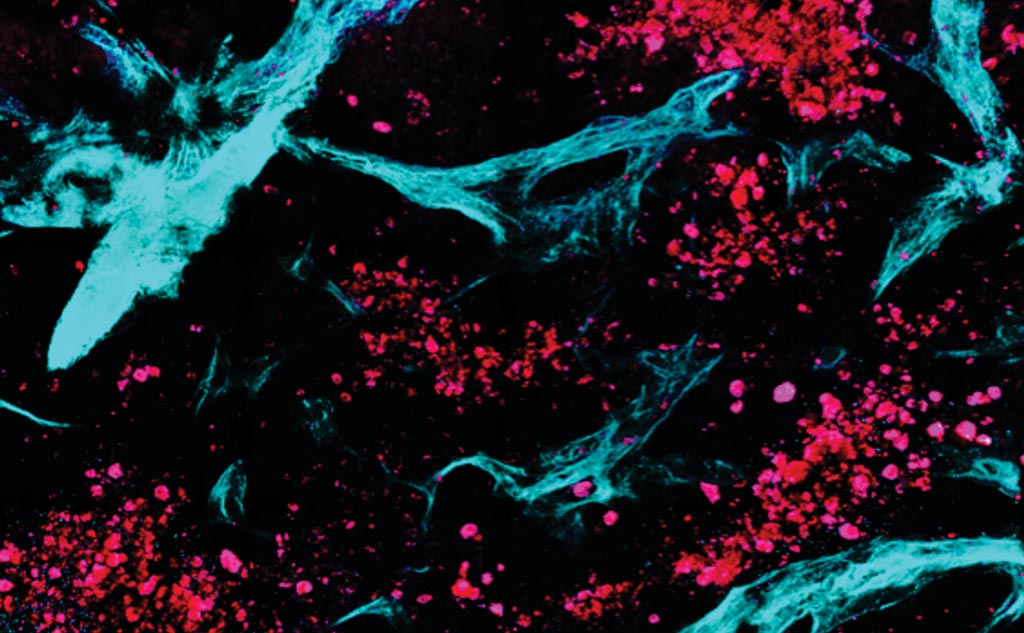
Ученые объединили многофотонную микроскопию с автоматизированными алгоритмами получения изображений и статистического анализа, чтобы различить здоровые и больные ткани. На этом изображении, полученном полностью без меток, неинвазивным способом, коллаген окрашен в зеленый цвет, а кластеры метастатических клеток яичников представлены в красном цвете (фото любезно предоставлено Университетом Тафтса).
Для больных раком наличие метастазов требует установления стадии, которая, в свою очередь, определяет соответствующий выбранный путь лечения. Для гинекологических злокачественных новообразований, таких как рак яичника, очень важно различать локализованный и метастатический статус заболевания, поскольку это значительным образом влияет на лечение.
Для диагностики in situ в режиме реального времени новые методы визуализации, которые предоставляют метаболическую и структурную информацию на клеточном и субклеточном уровне, могут быть очень полезны, особенно с учетом того, что эти методы все больше внедряются в зонды и микроэндоскопы, которые обеспечивают интравитальный доступ к органам, расположенным глубоко в теле.
Ученые-биомедики из Университета Тафтса (Медфорд, штат Массачусетс, США) и их коллеги взяли образцы у восьми пациентов, которым была сделана открытая лапаротомия в рамках обычной медицинской помощи. После завершения всех интраабдоминальных процедур в ходе операции у каждого пациента было взято восемь биопсий здоровой париетальной брюшины и, при их наличии, четырех метастазов из париетальной области. Все пораженные участки были оценены патологом с использованием стандартной гистологии с окраской гематоксилином и эозином.
Ткани были визуализированы с использованием многофотонного лазерного сканирующего микроскопа для создания изображений собственной флуоресценции и изображений генерации второй гармоники (ГВГ) при возбуждении на длинах волн 755 нм и 900 нм соответственно, с излучением сигнала, полученным на 460±20 и 525±25 нм. Свет лазера фокусировался на образце с использованием объектива с 25-кратным увеличением (0,9 NA/водная иммерсия), а нейтральные фильтры использовались для достижения мощности 25–35 мВт. Для каждой ткани были оценены не менее двух-трех случайных полей, что позволило получить в общей сложности 30 и 11 изображений для групп тканей здоровой и метастатической биопсии соответственно (512 × 512 пикселей, поле зрения 600 микрон, разрешение 1,17 микрона на пиксель). Изображения были сфокусированы на глубине ~20-100 мкм от мезотелиальной поверхности тканей.
Команда обнаружила, что здоровые ткани демонстрируют большие различия в контрасте и корреляционных характеристиках в зависимости от расстояния, что соответствует повторяющимся, увеличенным локальным колебаниям интенсивности. На изображениях метастатической ткани наблюдалось снижение контрастности и соответствующих корреляционных значений, более однородная картина интенсивности и более мелкие волокна, что указывает на разрушение здоровой стромы раковым инфильтратом. Анализируя 41 изображение, полученное с помощью биопсии, методика правильно классифицировала 40 из 41 изображения (точность 97,5%). В общей сложности 11 образцов были правильно классифицированы как метастатические (чувствительность 100%), а 29 из 30 были правильно классифицированы как здоровые (специфичность 96,6%).
Димитра Поли (Dimitra Pouli), доктор медицины, врач-ординатор в области патологии и соавтор исследования, говорит: “Метод, использованный в этой работе, идентифицирует клеточные и тканевые особенности полностью без меток на микроскопическом уровне, по сути действуя как биопсия без ножа”. Исследование было опубликовано в августовском выпуске журнала Biomedical Optics Express за 2019 год.
Ссылки по теме:
Tufts University
Для диагностики in situ в режиме реального времени новые методы визуализации, которые предоставляют метаболическую и структурную информацию на клеточном и субклеточном уровне, могут быть очень полезны, особенно с учетом того, что эти методы все больше внедряются в зонды и микроэндоскопы, которые обеспечивают интравитальный доступ к органам, расположенным глубоко в теле.
Ученые-биомедики из Университета Тафтса (Медфорд, штат Массачусетс, США) и их коллеги взяли образцы у восьми пациентов, которым была сделана открытая лапаротомия в рамках обычной медицинской помощи. После завершения всех интраабдоминальных процедур в ходе операции у каждого пациента было взято восемь биопсий здоровой париетальной брюшины и, при их наличии, четырех метастазов из париетальной области. Все пораженные участки были оценены патологом с использованием стандартной гистологии с окраской гематоксилином и эозином.
Ткани были визуализированы с использованием многофотонного лазерного сканирующего микроскопа для создания изображений собственной флуоресценции и изображений генерации второй гармоники (ГВГ) при возбуждении на длинах волн 755 нм и 900 нм соответственно, с излучением сигнала, полученным на 460±20 и 525±25 нм. Свет лазера фокусировался на образце с использованием объектива с 25-кратным увеличением (0,9 NA/водная иммерсия), а нейтральные фильтры использовались для достижения мощности 25–35 мВт. Для каждой ткани были оценены не менее двух-трех случайных полей, что позволило получить в общей сложности 30 и 11 изображений для групп тканей здоровой и метастатической биопсии соответственно (512 × 512 пикселей, поле зрения 600 микрон, разрешение 1,17 микрона на пиксель). Изображения были сфокусированы на глубине ~20-100 мкм от мезотелиальной поверхности тканей.
Команда обнаружила, что здоровые ткани демонстрируют большие различия в контрасте и корреляционных характеристиках в зависимости от расстояния, что соответствует повторяющимся, увеличенным локальным колебаниям интенсивности. На изображениях метастатической ткани наблюдалось снижение контрастности и соответствующих корреляционных значений, более однородная картина интенсивности и более мелкие волокна, что указывает на разрушение здоровой стромы раковым инфильтратом. Анализируя 41 изображение, полученное с помощью биопсии, методика правильно классифицировала 40 из 41 изображения (точность 97,5%). В общей сложности 11 образцов были правильно классифицированы как метастатические (чувствительность 100%), а 29 из 30 были правильно классифицированы как здоровые (специфичность 96,6%).
Димитра Поли (Dimitra Pouli), доктор медицины, врач-ординатор в области патологии и соавтор исследования, говорит: “Метод, использованный в этой работе, идентифицирует клеточные и тканевые особенности полностью без меток на микроскопическом уровне, по сути действуя как биопсия без ножа”. Исследование было опубликовано в августовском выпуске журнала Biomedical Optics Express за 2019 год.
Ссылки по теме:
Tufts University
Latest Патология News
Channels
Clinical Chemistry
view channel
3D Printed Point-Of-Care Mass Spectrometer Outperforms State-Of-The-Art Models
Mass spectrometry is a precise technique for identifying the chemical components of a sample and has significant potential for monitoring chronic illness health states, such as measuring hormone levels... Read more.jpg)
POC Biomedical Test Spins Water Droplet Using Sound Waves for Cancer Detection
Exosomes, tiny cellular bioparticles carrying a specific set of proteins, lipids, and genetic materials, play a crucial role in cell communication and hold promise for non-invasive diagnostics.... Read more
Highly Reliable Cell-Based Assay Enables Accurate Diagnosis of Endocrine Diseases
The conventional methods for measuring free cortisol, the body's stress hormone, from blood or saliva are quite demanding and require sample processing. The most common method, therefore, involves collecting... Read moreMolecular Diagnostics
view channel.jpg)
New Respiratory Syndromic Testing Panel Provides Fast and Accurate Results
Respiratory tract infections are a major reason for emergency department visits and hospitalizations. According to the CDC, the U.S. sees up to 41 million influenza cases annually, resulting in several... Read more
New Synthetic Biomarker Technology Differentiates Between Prior Zika and Dengue Infections
Until now, researchers and clinicians have lacked diagnostic tools to easily differentiate between past infections with different flaviviruses—a family of mostly mosquito- and tick-borne viruses that include... Read moreHematology
view channel
Next Generation Instrument Screens for Hemoglobin Disorders in Newborns
Hemoglobinopathies, the most widespread inherited conditions globally, affect about 7% of the population as carriers, with 2.7% of newborns being born with these conditions. The spectrum of clinical manifestations... Read more
First 4-in-1 Nucleic Acid Test for Arbovirus Screening to Reduce Risk of Transfusion-Transmitted Infections
Arboviruses represent an emerging global health threat, exacerbated by climate change and increased international travel that is facilitating their spread across new regions. Chikungunya, dengue, West... Read more
POC Finger-Prick Blood Test Determines Risk of Neutropenic Sepsis in Patients Undergoing Chemotherapy
Neutropenia, a decrease in neutrophils (a type of white blood cell crucial for fighting infections), is a frequent side effect of certain cancer treatments. This condition elevates the risk of infections,... Read more
First Affordable and Rapid Test for Beta Thalassemia Demonstrates 99% Diagnostic Accuracy
Hemoglobin disorders rank as some of the most prevalent monogenic diseases globally. Among various hemoglobin disorders, beta thalassemia, a hereditary blood disorder, affects about 1.5% of the world's... Read moreImmunology
view channel
Diagnostic Blood Test for Cellular Rejection after Organ Transplant Could Replace Surgical Biopsies
Transplanted organs constantly face the risk of being rejected by the recipient's immune system which differentiates self from non-self using T cells and B cells. T cells are commonly associated with acute... Read more
AI Tool Precisely Matches Cancer Drugs to Patients Using Information from Each Tumor Cell
Current strategies for matching cancer patients with specific treatments often depend on bulk sequencing of tumor DNA and RNA, which provides an average profile from all cells within a tumor sample.... Read more
Genetic Testing Combined With Personalized Drug Screening On Tumor Samples to Revolutionize Cancer Treatment
Cancer treatment typically adheres to a standard of care—established, statistically validated regimens that are effective for the majority of patients. However, the disease’s inherent variability means... Read moreMicrobiology
view channel
Integrated Solution Ushers New Era of Automated Tuberculosis Testing
Tuberculosis (TB) is responsible for 1.3 million deaths every year, positioning it as one of the top killers globally due to a single infectious agent. In 2022, around 10.6 million people were diagnosed... Read more
Automated Sepsis Test System Enables Rapid Diagnosis for Patients with Severe Bloodstream Infections
Sepsis affects up to 50 million people globally each year, with bacteraemia, formerly known as blood poisoning, being a major cause. In the United States alone, approximately two million individuals are... Read moreEnhanced Rapid Syndromic Molecular Diagnostic Solution Detects Broad Range of Infectious Diseases
GenMark Diagnostics (Carlsbad, CA, USA), a member of the Roche Group (Basel, Switzerland), has rebranded its ePlex® system as the cobas eplex system. This rebranding under the globally renowned cobas name... Read more
Clinical Decision Support Software a Game-Changer in Antimicrobial Resistance Battle
Antimicrobial resistance (AMR) is a serious global public health concern that claims millions of lives every year. It primarily results from the inappropriate and excessive use of antibiotics, which reduces... Read morePathology
view channelHyperspectral Dark-Field Microscopy Enables Rapid and Accurate Identification of Cancerous Tissues
Breast cancer remains a major cause of cancer-related mortality among women. Breast-conserving surgery (BCS), also known as lumpectomy, is the removal of the cancerous lump and a small margin of surrounding tissue.... Read more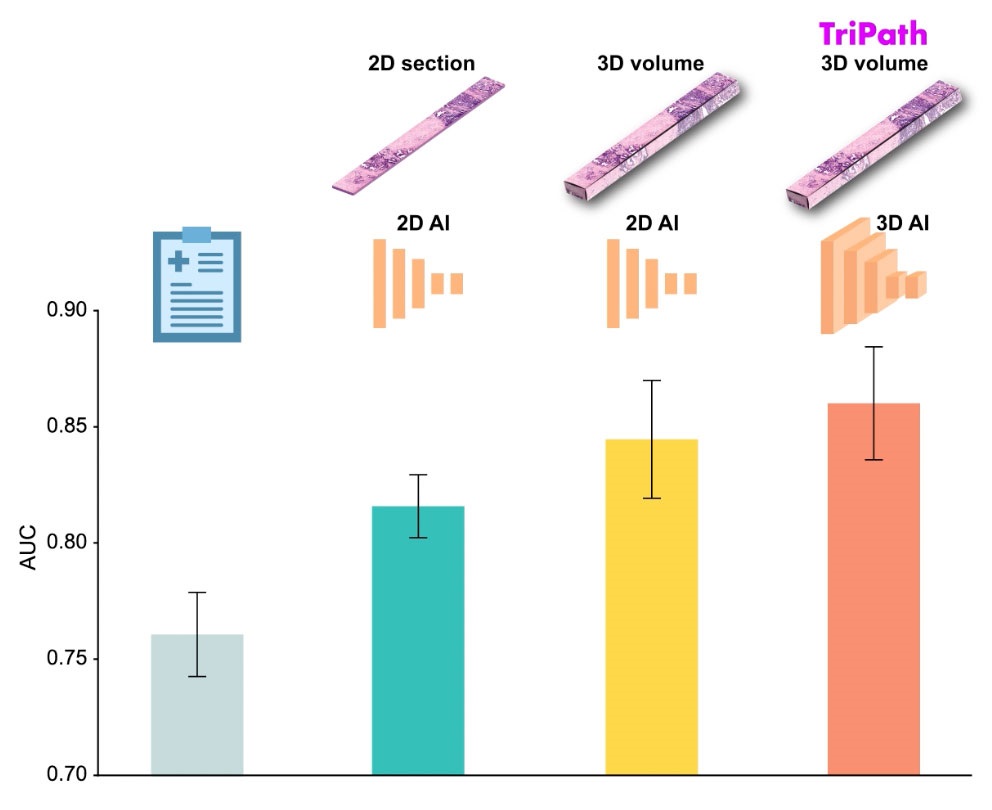
AI Advancements Enable Leap into 3D Pathology
Human tissue is complex, intricate, and naturally three-dimensional. However, the thin two-dimensional tissue slices commonly used by pathologists to diagnose diseases provide only a limited view of the... Read more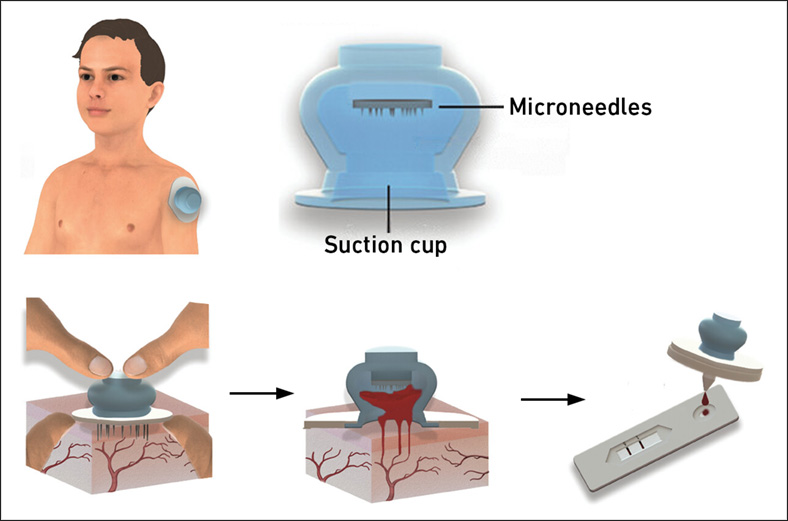
New Blood Test Device Modeled on Leeches to Help Diagnose Malaria
Many individuals have a fear of needles, making the experience of having blood drawn from their arm particularly distressing. An alternative method involves taking blood from the fingertip or earlobe,... Read more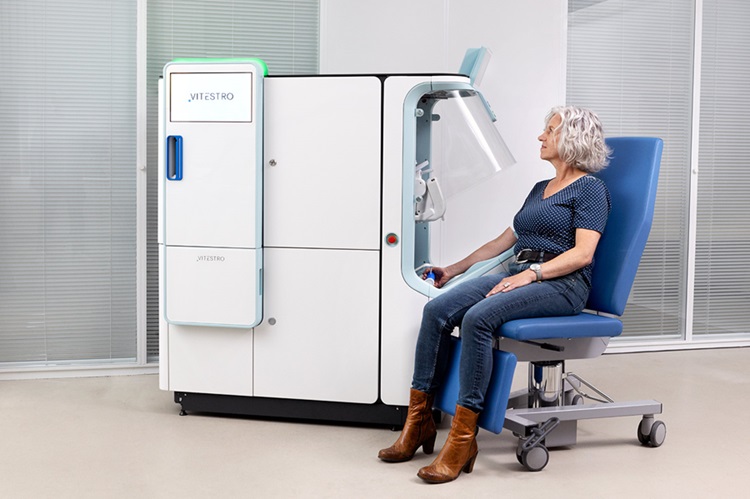
Robotic Blood Drawing Device to Revolutionize Sample Collection for Diagnostic Testing
Blood drawing is performed billions of times each year worldwide, playing a critical role in diagnostic procedures. Despite its importance, clinical laboratories are dealing with significant staff shortages,... Read moreTechnology
view channel
New Diagnostic System Achieves PCR Testing Accuracy
While PCR tests are the gold standard of accuracy for virology testing, they come with limitations such as complexity, the need for skilled lab operators, and longer result times. They also require complex... Read more
DNA Biosensor Enables Early Diagnosis of Cervical Cancer
Molybdenum disulfide (MoS2), recognized for its potential to form two-dimensional nanosheets like graphene, is a material that's increasingly catching the eye of the scientific community.... Read more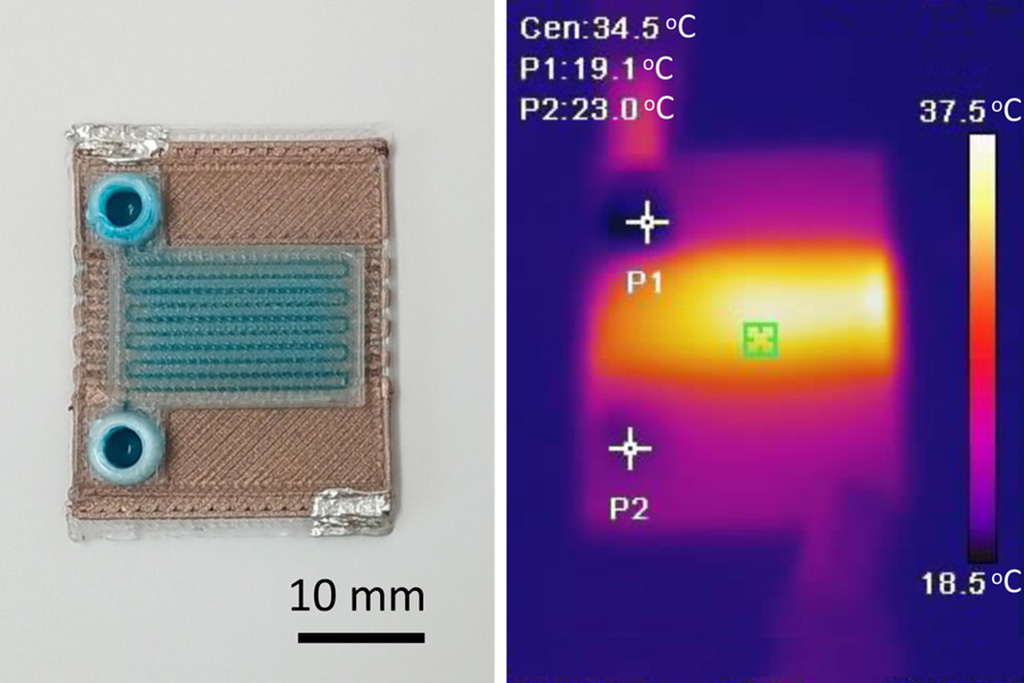
Self-Heating Microfluidic Devices Can Detect Diseases in Tiny Blood or Fluid Samples
Microfluidics, which are miniature devices that control the flow of liquids and facilitate chemical reactions, play a key role in disease detection from small samples of blood or other fluids.... Read more
Breakthrough in Diagnostic Technology Could Make On-The-Spot Testing Widely Accessible
Home testing gained significant importance during the COVID-19 pandemic, yet the availability of rapid tests is limited, and most of them can only drive one liquid across the strip, leading to continued... Read moreIndustry
view channel
Danaher and Johns Hopkins University Collaborate to Improve Neurological Diagnosis
Unlike severe traumatic brain injury (TBI), mild TBI often does not show clear correlations with abnormalities detected through head computed tomography (CT) scans. Consequently, there is a pressing need... Read more
Beckman Coulter and MeMed Expand Host Immune Response Diagnostics Partnership
Beckman Coulter Diagnostics (Brea, CA, USA) and MeMed BV (Haifa, Israel) have expanded their host immune response diagnostics partnership. Beckman Coulter is now an authorized distributor of the MeMed... Read more_1.jpg)