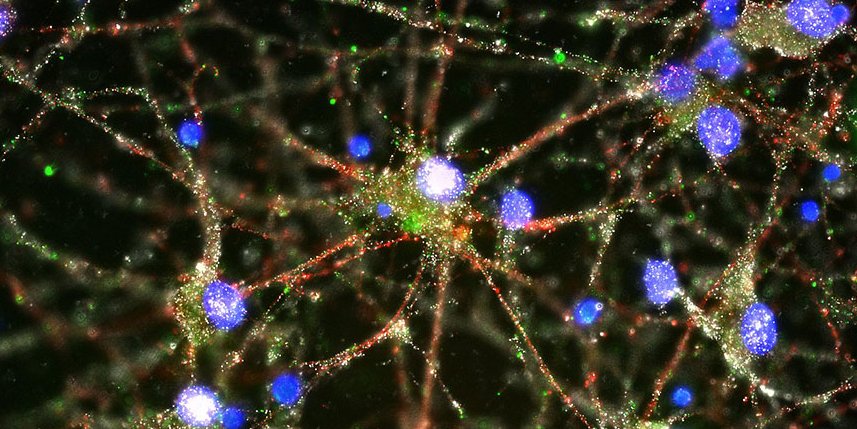
Впервые рассмотрен ген, который может объяснить биологическое происхождение шизофрении
By LabMedica International staff writers
Posted on 11 Feb 2016
В исследовании, представляющем собой историческую значимость, научные сотрудники определили мутации гена компонента системы комплемента С4, которые в значительной степени связаны с риском развития шизофрении.Posted on 11 Feb 2016
В дальнейшем было обнаружено, что C4, хорошо известный белок иммунной системы, также задействован в синаптическом прунинге в головном мозге. Исследование дает важное представление о биологическом происхождении и лежащей в основе физиологии этой изнурительной болезни и, вероятно, поможет в поисках нового пути для разработки диагностических тестов для раннего обнаружения заболевания, а также более эффективных лекарственных препаратов для лечения и профилактики, что позволит направить терапевтические стратегии на устранение причин нарушения, а не его симптомов.
“В связи с тем, что шизофрения была впервые описана более века тому назад, природа заболевания оставалась своего рода «черным ящиком», отчасти потому что было практически невозможно смоделировать нарушение в клетках или у животных, — сказал руководитель исследования Стивен МакКэрролл (Steven McCarroll), адъюнкт-профессор в Гарвардской медицинской школе и руководитель отдела генетики в Центре психиатрических исследований Стэнли при Институте Брода (Кембридж, штат Массачусетс, США). – Геном человека обеспечивает эффективный новый путь к пониманию этой болезни”.
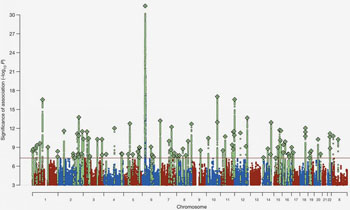
В прошлые годы были определены более 100 областей в геноме человека, которые несут факторы риска возникновения шизофрении. Наиболее сильный связанный с риском сигнал был, вне всяких сомнений, на хромосоме 6, в области, долгое время ассоциировавшейся с инфекционным заболеванием, заставляя некоторых предполагать, что шизофрения могла бы быть вызвана возбудителем инфекции.
Наиболее выраженная из известных генетическая связь шизофрении на уровне численности популяции заключается в изменчивости в локусе главного комплекса гистосовместимости иммунной системы. Однако гены и молекулярные механизмы, являющиеся причиной этого процесса, остаются трудными для понимания при использовании обычных генетических методов. Новое исследование показывает, что эта связь в некоторой степени обусловлена множеством разнообразных аллелей генов C4. Изучая уровни РНК, исследователи обнаружили, что эти аллели приводят к значительному изменению уровней экспрессии C4A и C4B в головном мозге.
Исследование было основано на изучении ДНК, взятой более чем у 100,000 человек из 30 стран, подробном анализе сложной генетической изменчивости в более чем 65,000 геномов человека, развитии инновационной аналитической стратегии, тщательном изучении образцов головного мозга сотен людей после их смерти и использовании данных об исследованиях на животных, чтобы в дальнейшем лучше понять биологическую функцию C4.
Анализ данных о геноме почти 65,000 человек (с шизофренией и без нее) показал поразительную корреляцию: пациенты, у которых оказались особые аллели C4, продемонстрировали более высокую экспрессию этих аллелей, а также более высокий риск развития шизофрении. Таким образом, мутации, приводящие к аномально повышенной экспрессии C4, были в значительной степени связаны с предрасположенностью к развитию шизофрении.
Каким образом компонент системы комплемента С4 (он, как известно, маркирует патогенные микроорганизмы для уничтожения иммуноцитами) влияет на риск возникновения шизофрении? Исследователи обнаружили, что белок человека C4 локализован в синапсах, дендритах, аксонах и телах нейронов. Они также обнаружили, что C4 играет ключевую роль в сокращении числа синапсов во время созревания головного мозга. В частности, C4 был необходим для того, чтобы компонент системы комплемента С3 накапливался в синапсах, подавая сигнал о том, что эти синапсы должны быть удалены. Факты также указывают на то, что более высокая активность C4 связана с увеличенным сокращением числа синапсов в головном мозге во время ключевого периода развития мозга. У мышей компонент системы комплемента С4 выступает посредником при уничтожении синапсов во время постнатального развития.
Человеческий мозг в норме претерпевает обширное сокращение синапсов (особенно в коре головного мозга) во время подросткового периода, характерного периода появления симптомов. “В норме сокращение избыточных нейронов избавляет от лишних связей, в которых мы больше не нуждаемся, адаптируя наш мозг для оптимальной работы, однако чрезмерный прунинг может ослабить психическую функцию, — объяснил Томас Ленер (Thomas Lehner), доктор философии, директор отдела по координации научно-исследовательской работы в области геномики в Национальном институте психического здоровья при Национальном институте здоровья (Бетесда, штат Мэриленд, США). — Это могло помочь объяснить время появления симптомов в конце подросткового периода/ старшем подростковом возрасте и уменьшение объемов функционирующей ткани головного мозга при шизофрении”. Результаты помогут также найти ответ на вопрос, почему люди с шизофренией обычно имеют более тонкую кору головного мозга с меньшим количеством синапсов, чем лица, не пораженные этим заболеванием.
Результаты показали, что чрезмерное сокращение числа синапсов в головном мозге создает предрасположенность к шизофрении. Благоприятным обстоятельством является то, что многое уже известно о роли C4 и других белков системы комплемента в иммунной системе, поэтому исследователи могут использовать по максимуму богатый выбор имеющихся знаний, чтобы определить возможные терапевтические методы. Например, антикомплементные лекарственные препараты уже разрабатываются для лечения других заболеваний.
“Несмотря на то, что еще рано делать какие-либо выводы, мы увидели эффективность понимания биологического механизма болезни в другом свете, - сказал Эрик Ландер (Eric Lander), директор Института Брода. – Понимание шизофрении будет таким же образом ускорять прогресс в работе, направленной на борьбу с этим тяжелым заболеванием, которое поражает молодых людей”.
Проведение работы стало возможным в значительной степени благодаря каталитическому финансированию от Центра Стэнли; данная научная работа посвящена покойному Теду Стэнли (Ted Stanley). “Филантропия помогла нам сделать ставки на рискованные научные исследования, результаты которых, возможно, будут меняться, — сказал директор Центра Стэнли Стивен Хайман (Steven Hyman). –Поддержка недавно почивших Теда и Вэды Стэнли (Vada Stanley) дала ученым Института Брода возможность собрать воедино человеческие ресурсы, технические возможности и материальные средства и направить их на развитие инновационных методов”.
“Данное исследование обозначает решающий поворотный момент в борьбе с психическим расстройством. Это меняет ход дела, - добавил Брюс Катберт (Bruce Cuthbert), доктор философии, исполняющий обязанности директора Национального института психического здоровья. – Благодаря этому важному научному открытию в области генетики мы можем наконец представить себе потенциальные возможности клинических исследований, раннего обнаружения болезни и даже профилактических мер”.
Исследование, проведенное Сейкаром Э. (Sekar A.) и соавторами, было опубликовано онлайн, накануне выхода в печать 27 января 2016 г. в журнале Nature.
Ссылки по теме:
Broad Institute
[US] National Institute of Mental Health (NIMH)
More about the study