Скрининговый набор ограждает пациентов от рака шейки матки и избыточного лечения
By LabMedica International staff writers
Posted on 01 Dec 2015
Новый набор клинически проверенных генетических и патологических тестов для скрининга и диагностики рака шейки матки (РШМ), вызываемого вирусом папилломы человека (ВПЧ), помогает выявить женщин с высоким риском развития этой в высшей степени предотвратимой болезни, которая по-прежнему классифицируется как 4-й по распространенности рак у женщин – 530 000 новых случаев в год, из которых около половины пациенток умирают.Posted on 01 Dec 2015
Новый набор для скрининга рака шейки матки (Cervical Cancer Screening Portfolio) от Roche (Базель, Швейцария) объединяет в себе различные анализы, чтобы оказать поддержку лабораториям и гинекологам в предоставлении оптимального ухода за пациентами, и является уникальным в том, что помогает обследовать, диагностировать и лечить больных. Большинство случаев РШМ наблюдается в странах, в которых еще не внедрен систематический скрининг. Введение систематического теста Папаниколау (Пап-мазка) для выявления предраковых поражений во многих странах помогло уменьшить число женщин, которые страдают или умирают от РШМ, по крайней мере на 80%. Хотя заболеваемость значительно сократилась в результате введения анализа Папаниколау, данные показали свои ограничения, вследствие чего до трети случаев РШМ возникают у женщин с нормальными результатами Пап-теста.
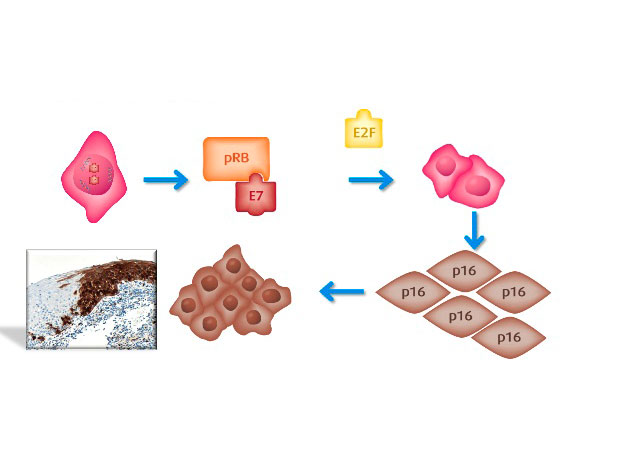
Скрининговый набор анализа рака шейки матки Cervical Cancer Screening Portfolio от Roche, иммуногистохимический анализ CINtec p16 Histology обнаруживает p16-INK4a в препаратах биопсии шейки матки. На рисунке показано, что в клетках с трансформирующей ВПЧ-инфекцией вирусный ВПЧ-онкобелок Е7 ухудшает функцию pRB, нарушая его способность связываться с E2F. Это приводит к пролиферации клеток, нерегулируемой генетической нестабильности и избыточной экспрессии p16, поддающейся обнаружению с помощью иммуногистохимического окрашивания (изображение предоставлено Ventana, Roche).
РШМ, вызванному хронической инфекцией ВПЧ, может потребоваться более 10-15 лет, прежде чем произойдет развитие в полномасштабную болезнь. Хотя от большинства из более чем 100 типов ВПЧ организм очищается естественным путем, типы ВПЧ с высоким риском вызывают 99% случаев РШМ, в 70% случаев их причиной являются два конкретных генотипа ВПЧ-16 и -18. Скрининг РШМ находится в переходной стадии, и технологии значительно продвинулись: инновационное молекулярное тестирование на основе 16/18 генотипирования ДНК ВПЧ, а также иммуноцитологическое и иммуногистологическое окрашивания для выявления p16-INK4a и Ki-67 имеют возможность различать женщин с наибольшим риском, женщин, которым требуется немедленное лечение из-за существующих нарушений, и женщин, которые могут спокойно вернуться к обычному скринингу. Это означает, что профилактические меры могут быть предприняты без задержки, потенциально спасая жизни за счет защиты женщин от бремени рака и его лечения.
Профилактическая практика развивается параллельно с техническим прогрессом. В нынешних руководящих принципах скрининга США совместное тестирование на ВПЧ в дополнение к тесту Папаниколау теперь предпочтительнее, чем один только Папаниколау-тест для женщин в возрасте 30-65 лет. Рекомендация основана на данных, что, по сравнению с одной только Пап-цитологией, добавление анализа на ВПЧ повышает уровень обнаружения (рака шейки матки и его предшественников) и снижает процент инвазивного РШМ. Интеграция ВПЧ-теста в первичный скрининг поможет защитить большее число женщин. После санкционирования в 2014 г. Управлением по контролю качества пищевых продуктов и лекарственных средств США (FDA) анализа Roche’s cobas HPV Test как автономного первичного скринингового теста, два профессиональных сообщества выпустили временное руководство по использованию в США первичного скрининга ВПЧ. Эти изменения отражают возрастающее принятие принципов первичного скрининга ВПЧ по всему миру.
ВПЧ-тест Cobas является единственным сертифицированным FDA и получившим СЕ-маркировку ВПЧ-тестом первичного скрининга первой линии для выявления женщин из группы риска. Из одного образца в одном тесте Cobas HPV одновременно определяет общий результат для 12 генотипов с высоким риском и предоставляет отдельные результаты для двух генотипов с самым высоким риском: HPV-16 и HPV-18. Это разделение позволяет более надежно определить риск каждого человека.
CINtec PLUS Cytology, иммуноцитохимический анализ для идентификации полного поражения шейки матки (CIN2+), является единственным тестом, который использует технологию двух биомаркеров для одновременного обнаружения p16-INK4a и Ki-67, чтобы обеспечить убедительный индикатор присутствия трансформирующей ВПЧ-инфекции. Тест используется в качестве инструмента для сортировки, позволяющей определить, какие женщины могут получить наибольшую пользу от кольпоскопии.
CINtec p16 Histology, иммуногистохимический анализ, выявляет биомаркер р16-Ink4a в препаратах биопсии шейки матки. Используемый в сочетании с препаратами, окрашенными гематоксилином и эозином (H&E), тест CINtec p16 Histology позволяет патологам точно и рационально диагностировать и подтверждать подозрения на болезни шейки матки и, таким образом, получать окончательные результаты, которые помогут принимать более обоснованные решения о последующем наблюдении за пациентом.
Клиническая проверка скринингового теста Roche на рак шейки матки
Cobas ВПЧ-тест: Масштабное исследование, включающее более чем 47 000 женщин в возрасте ≥21 лет, проходящих обычный скрининг РШМ, клинически утвердило тест cobas HPV Test для всех причастных групп населения: совместное тестирование посредством ASC-US-цитологии, ВПЧ- и Пап-анализа и основного скрининга. Это исследование было также крупнейшим перспективным скрининговым исследованием РШМ для оценки клинического использования ДНК ВПЧ-тестирования с 16/18 генотипированием. Опубликованное под названием ATHENA (Addressing THE Need for Advanced HPV diagnostics – “Обращение к необходимости совершенствования диагностики ВПЧ”) в нескольких отчетах в ведущих научных журналах, исследование является крупнейшим поворотным исследованием ВПЧ среди когда-либо проведенных на сегодняшний день. В дополнение к ATHENA были опубликованы другие исследования, в том числе результаты двух успешных европейских проверок теста в рамках широко распространенных европейских критериев анализа ВПЧ. Кроме того, ВПЧ-тест cobas HPV Test был одобрен FDA в апреле 2011 года для проработки неоднозначных Пап-цитологий (ASC-US-сортировка) и ВПЧ и совместного Пап-скрининга по содержательности данных ATHENA. Далее, в апреле 2014 года, последовала сертификация FDA для автономного первичного скрининга ВПЧ у женщин в возрасте от 25 лет и выше.
Цитология CINtec PLUS и гистология CINtec p16 Histology: Оба испытания имеют широкомасштабные клинические подтверждения в поддержку их применения для скрининга и диагностики.
При использовании в качестве сортировки ВПЧ-тестирования, цитология CINtec PLUS Cytology продемонстрировала высокую чувствительность и специфичность в выявлении ≥CIN2 поражений, таким образом избегая лишней кольпоскопии. Кроме того, для пациентов в возрасте 30 лет и старше, с нормальными результатами Пап-цитологии, но положительных на ВПЧ, CINtec PLUS Cytology можете добавить пользу за счет выявления лежащей в основе ≥CIN2.
В диагностике предрака шейки матки дополнительное применение гистологического теста CINtec p16 Histology повышало чувствительность обнаружения CIN3 на 11% по сравнению с одним только окрашиванием H&E. Процент ложноотрицательных результатов был снижен на 45% из-за значительно повышенной точности при использовании CINtec p16 Histology в сочетании с H&E. Тест также может выявлять повреждения, ранее пропущенные при использовании только H&E. LAST Working Group рекомендует использовать биомаркер р16-INK4a в качестве дополнения к H&E-диагностике как единственный биомаркер с достаточным количеством подтверждений – данные рекомендации впоследствии были приняты в нормативах Всемирной организации здравоохранения (ВОЗ).
Ссылки по теме:
Roche
Roche Cervical Cancer Prevention Portfolio