Анализ крови обнаруживает генетические мутации при раке легких
By LabMedica International staff writers
Posted on 29 Apr 2016
Простой анализ крови может быстро и точно обнаружить мутации в двух основных генах при немелкоклеточных опухолях легких, демонстрируя потенциал теста в качестве клинического инструмента для выявления пациентов, которые могут получить положительный результат от лекарственных препаратов, направленных на борьбу с данными мутациями.Posted on 29 Apr 2016
Немелкоклеточные опухоли легких являются наиболее распространенной формой рака легких, которые обнаруживаются более чем у 200,000 человек в США каждый год. Приблизительно 30% пациентов с немелкоклеточным раком легких имеют мутации в одном из генов, включенных в недавно проведенное исследование, и часто могут проходить лечение с использованием методов таргетной терапии.
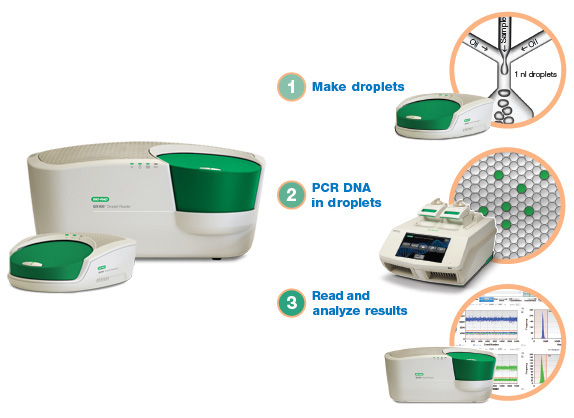
Система для проведения капельной цифровой полимеразной цепной реакции (фото любезно предоставлено Bio-Rad Laboratories).
Врачи-онкологи в Онкологическом институте Дана-Фарбера (Бостон, штат Массачусетс, США) и их коллеги в плановом порядке включили в исследование 180 пациентов с немелкоклеточным раком легких, из которых у 120-ти болезнь была впервые диагностирована, а у 60-ти возникла устойчивость к предыдущему лечению, что позволило болезни повториться. Бесклеточная ДНК участников исследования была проверена на мутации в генах рецептора эпидермального фактора роста (EGFR) и гомолога вирусного онкогена саркомы крыс Кирстен (KRAS), а также на отдельную мутацию в EGFR, которая позволяет опухолевым клеткам становиться устойчивыми к первой линии лекарственных препаратов направленного действия.
Тест был выполнен с использованием технологии, известной как капельная цифровая полимеразная цепная реакция (ПЦР) (Bio-Rad; Геркулес, штат Калифорния, США), которая вычисляет количество отдельных символов генетического кода в бесклеточной ДНК, чтобы определить, присутствуют ли характерные мутации. Каждому участнику также была проведена обычная биопсия ткани, чтобы проверить на наличие тех же самых мутаций. Затем результаты жидких биопсий сравнили с результатами биопсий ткани. Время выполнения генотипирования тканей было измерено от даты предварительного генотипирования до сообщения заключительного результата генотипирования.
Данные показали, что жидкие биопсии обеспечивали результаты намного быстрее. Среднее время выполнения жидких биопсий составляло 3 дня, по сравнению с 12 днями, необходимыми для выполнения биопсий ткани пациентам, у которых болезнь была впервые диагностирована, и 27 днями для больных, устойчивых к действию лекарственных препаратов. Также было определено, что жидкая биопсия является очень точной. У пациентов с впервые диагностированным заболеванием прогностическая ценность капельной цифровой ПЦР плазмы крови составляла 100% для первичной мутации EGFR и мутации KRAS, означая, что пациент, который получил положительный результат теста на любую мутацию, должен был точно иметь данную мутацию в своей опухоли. Для пациентов с мутацией EGFR, связанной с устойчивостью, прогностическая ценность капельного цифрового ПЦР-анализа составляла 79%, и это позволяет предположить, что анализ крови смог обнаружить новые случаи заболевания вследствие мутации, которые были пропущены при использовании стандартного метода проведения биопсий.
Доктор Линетт Шолл (Lynette Sholl), патолог, сказала: “Данные исследования являются убедительными. Мы проверили полученные авторами данные результатов исследования путем перекрестного сравнения результатов жидких биопсий и биопсий ткани у 34 больных немелкоклеточным раком легких. Чтобы использоваться в качестве реального клинического теста, жидкая биопсия должна обеспечивать надежные, точные данные и быть практичной с точки зрения логистики. Это как раз было продемонстрировано при использовании анализа крови, основанного на капельной цифровой ПЦР. Тест имеет большую практическую ценность и для пациентов, у которых немелкоклеточный рак легких был впервые диагностирован, и для тех, у кого произошел рецидив заболевания. Он экономит время и позволяет провести количественную оценку, поскольку указывает на количество мутировавшей ДНК в образце, что может быть легко использовано в центрах лечения рака”.
Исследование было опубликовано 7 апреля 2016 года в журнале JAMA Oncology.
Ссылки по теме:
Dana-Farber Cancer Institute
Bio-Rad