Анализ крови позволяет улучшить лечение острого миелобластного лейкоза
By LabMedica International staff writers
Posted on 09 Mar 2016
Разработан простой анализ крови, который способен обнаруживать остаточные уровни лейкозных клеток, сохранившихся после интенсивной химиотерапии. Анализ может дать прогноз, кто из пациентов с острым миелобластным лейкозом подвержен риску повторения заболевания в будущем, и это поможет ориентировать врачей на принятие дальнейших решений о лечении. Posted on 09 Mar 2016
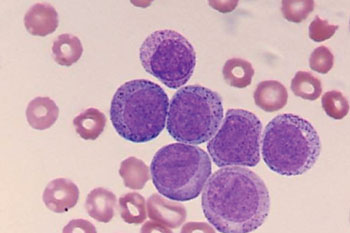
Острый миелобластный лейкоз представляет собой тип рака крови, который диагностируют приблизительно у 2,400 человек каждый год в Великобритании, при этом пятилетняя выживаемость чрезвычайно низка: в живых остается меньше 2 из 10 пациентов. Лейкоз может быть вылечен у пациентов, которые в состоянии вынести интенсивное лечение, при этом прогноз у таких пациентов лучше.
Многочисленная команда ученых во главе с коллегами из Национального института исследований в области здравоохранения Великобритании (Лондон, Великобритания) провела с 6 апреля 2009 года по 31 декабря 2014 года исследование пациентов. Централизованный молекулярный скрининг позволил определить пациентов с мутациями в гене нуклеофосмина ( nucleophosmin, NPM1). Последующие образцы планировалось получать во время восстановления формулы крови после каждого цикла лечения и затем ежеквартально вплоть до 24 месяцев после консолидации ремиссии. Образцы, которые были получены в начальные моменты времени (т.е. во время восстановления после циклов индукции и консолидации), представляли собой преимущественно образцы периферической крови, так как для оценки костного мозга предпочтение было отдано проточной цитометрии.
Команда ученых определила минимальную остаточную болезнь при выполнении количественной полимеразной цепной реакции (ПЦР) с обратной транскриптазой, используя специфический праймер для обнаружения мутации со стандартным праймером и зондом. Анализы были выполнены в трёх параллельных подходах на платформе ABI 7900 (компания Applied Biosystems; Фостер-Сити, штат Калифорния, США), и уровни мутировавших транскриптов сравнили с экспрессией референсного гена с помощью плазмидных стандартов и метода определения разности значений пороговых циклов, используемого для редких мутаций. Высокопроизводительное секвенирование с применением набора HaloPlex Target Enrichment (компания Agilent Technologies; Санта-Клара, штат Калифорния, США) было выполнено на системе HiSeq 2000 (Компания Illumina; Сан-Диего, штат Калифорния, США).
Ученые обнаружили, что показатели при исследовании минимальной остаточной болезни были намного лучше при прогнозировании рецидива по сравнению с существующими методами, которые в основном учитывают генетические аномалии в пределах раковых клеток, влияющие на то, представляют они “высокий риск” или “низкий риск” у отдельных пациентов в начале лечения. Исследование минимальной остаточной болезни позволяет определить, находится ли пациент в состоянии “молекулярной ремиссии”, когда ничто не указывает на наличие дефектных генов, являющихся признаком присутствия лейкозных клеток в крови пациентов. Пациенты заболевали повторно в течение трех лет в 82% случаев, в которых исследование минимальной остаточной болезни обнаружило присутствие гена NPM1 в образце крови, взятом после первоначального лечения. Только у 30% пациентов, у которых не было поддающихся обнаружению лейкозных клеток в крови на данном этапе, случался рецидив в течение того же промежутка времени.
Дэвид Гримвэйд (David Grimwade), доктор философии, преподаватель и ведущий руководитель исследования, сказал: “Обычные методы для ведения лечения этого типа лейкемии являются неудовлетворительными. Исследование минимальной остаточной болезни является бесценным методом для мониторинга эффективности лечения и для определения пациентов, для которых использования химиотерапии не достаточно и которым требуется трансплантация стволовых клеток или новые методы лечения”. Исследование было опубликовано 20 января 2016 года в журнале The New England Journal of Medicine (NEJM).
Ссылки по теме:
UK National Institute for Health Research
Applied Biosystems
Agilent Technologies