Анализ капли крови позволит осуществлять мониторинг устойчивости к противомалярийным препаратам
|
By LabMedica International staff writers Posted on 04 Jul 2019 |
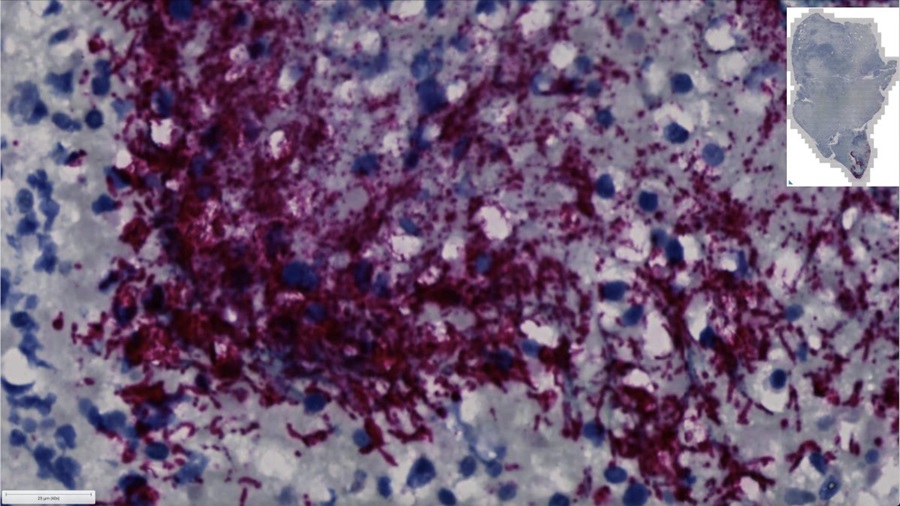
![Цветная электронная микрофотография, показывающая малярийного паразита (справа, синего цвета), сцепленного с эритроцитом человека. На вставке показан фрагмент точки контакта при большем увеличении (фото любезно предоставлено [США] NIAID через Wikimedia Commons). Цветная электронная микрофотография, показывающая малярийного паразита (справа, синего цвета), сцепленного с эритроцитом человека. На вставке показан фрагмент точки контакта при большем увеличении (фото любезно предоставлено [США] NIAID через Wikimedia Commons).](https://globetechcdn.com/mobile_labmedica/images/stories/articles/article_images/2019-07-04/2019_06_24_2019_06_25_labmedica_molecular-diagnostics_294778404_3263.jpg)
Цветная электронная микрофотография, показывающая малярийного паразита (справа, синего цвета), сцепленного с эритроцитом человека. На вставке показан фрагмент точки контакта при большем увеличении (фото любезно предоставлено [США] NIAID через Wikimedia Commons).
Разработан новый метод анализа ДНК непосредственно по капле крови, который поможет осуществлять мониторинг развития устойчивости к противомалярийным препаратам.
Мониторинг устойчивости к противомалярийным препаратам у паразита Plasmodium falciparum важен для предотвращения дальнейшего распространения заболевания, но доступные варианты оценки устойчивости обычно не применимы в полевых условиях. Молекулярное обнаружение, по всей видимости, является наиболее эффективным методом, но при этом оно также является наиболее сложным, поскольку требует выделения ДНК и использования инструментария ПЦР.
Чтобы разработать методику, более подходящую для использования за пределами традиционной лаборатории, исследователи из Университета Вандербильта (Нэшвилл, штат Теннесси, США) создали новые тесты, которые при использовании в сочетании с толерантной к ингибитору Taq-полимеразой (inhibitor-tolerant Taq polymerase) позволили генотипировать однонуклеотидный полиморфизм непосредственно из цельной крови. Фермент Taq-полимераза представляет собой термостабильную ДНК-полимеразу I, получившую название от термофильной бактерии Thermus aquaticus, из которой он был первоначально выделен. Он часто используется в полимеразной цепной реакции (ПЦР) – методе, направленном на значительное увеличение количества коротких сегментов ДНК.
Новые тесты имеют два ключевых конструктивных элемента: запертые нуклеиновые кислоты для повышения специфичности и репортерные красители Cy5 и TEX615, которые имеют меньшее оптическое перекрытие со спектрами поглощения крови, чем другие обычно используемые красители. Эффективность тестов была проверена на традиционном лабораторном приборе, а затем они были дополнительно протестированы на применяемой в полевых условиях методике адаптивной ПЦР.
Адаптивная ПЦР представляет собой ранее описанную платформу для ПЦР в реальном времени, использующую добавление левозакрученной ДНК (Z-ДНК) для контроля протекания реакции с целью большей результативности в месте оказания медицинской помощи. Этот метод оказался существенно проще и надежнее, чем традиционная ПЦР. Он функционирует за счет динамического управления термоциклированием посредством прямого мониторинга двух ключевых событий гибридизации – отжига праймера и плавления продукта во время реакции.
Результаты, полученные в ходе исследования, показали, что тесты позволяют различать P. falciparum дикого типа и хлорохин-резистентного мутанта в присутствии 2% крови. Эта стратегия значительно упростила выявление однонуклеотидного полиморфизма и предоставила более доступную альтернативу для наблюдения за устойчивостью к малярии в полевых условиях.
“Чтобы облегчить ингибирование компонентами крови, мы реконструировали молекулярные технологии, используемые для анализа ДНК. Мы применили репортерные красители, более оптически совместимые с кровью, в сочетании с определенным типом подгруппы ДНК для точного определения мутаций. Конечным результатом является анализ, в котором кровь непосредственно добавляется в реакционную пробирку для выявления мутаций, связанных с устойчивостью к противомалярийным лекарственным препаратам”, — говорит старший автор исследования доктор Фредерик Р. Хазелтон (Frederick R. Haselton), профессор биомедицинской инженерии и химии в Университете Вандербильта.
Исследование устойчивости к малярии было опубликовано в интернет-издании Journal of Molecular Diagnostics от 13 июня 2019 года.
Ссылки по теме:
Vanderbilt University
Мониторинг устойчивости к противомалярийным препаратам у паразита Plasmodium falciparum важен для предотвращения дальнейшего распространения заболевания, но доступные варианты оценки устойчивости обычно не применимы в полевых условиях. Молекулярное обнаружение, по всей видимости, является наиболее эффективным методом, но при этом оно также является наиболее сложным, поскольку требует выделения ДНК и использования инструментария ПЦР.
Чтобы разработать методику, более подходящую для использования за пределами традиционной лаборатории, исследователи из Университета Вандербильта (Нэшвилл, штат Теннесси, США) создали новые тесты, которые при использовании в сочетании с толерантной к ингибитору Taq-полимеразой (inhibitor-tolerant Taq polymerase) позволили генотипировать однонуклеотидный полиморфизм непосредственно из цельной крови. Фермент Taq-полимераза представляет собой термостабильную ДНК-полимеразу I, получившую название от термофильной бактерии Thermus aquaticus, из которой он был первоначально выделен. Он часто используется в полимеразной цепной реакции (ПЦР) – методе, направленном на значительное увеличение количества коротких сегментов ДНК.
Новые тесты имеют два ключевых конструктивных элемента: запертые нуклеиновые кислоты для повышения специфичности и репортерные красители Cy5 и TEX615, которые имеют меньшее оптическое перекрытие со спектрами поглощения крови, чем другие обычно используемые красители. Эффективность тестов была проверена на традиционном лабораторном приборе, а затем они были дополнительно протестированы на применяемой в полевых условиях методике адаптивной ПЦР.
Адаптивная ПЦР представляет собой ранее описанную платформу для ПЦР в реальном времени, использующую добавление левозакрученной ДНК (Z-ДНК) для контроля протекания реакции с целью большей результативности в месте оказания медицинской помощи. Этот метод оказался существенно проще и надежнее, чем традиционная ПЦР. Он функционирует за счет динамического управления термоциклированием посредством прямого мониторинга двух ключевых событий гибридизации – отжига праймера и плавления продукта во время реакции.
Результаты, полученные в ходе исследования, показали, что тесты позволяют различать P. falciparum дикого типа и хлорохин-резистентного мутанта в присутствии 2% крови. Эта стратегия значительно упростила выявление однонуклеотидного полиморфизма и предоставила более доступную альтернативу для наблюдения за устойчивостью к малярии в полевых условиях.
“Чтобы облегчить ингибирование компонентами крови, мы реконструировали молекулярные технологии, используемые для анализа ДНК. Мы применили репортерные красители, более оптически совместимые с кровью, в сочетании с определенным типом подгруппы ДНК для точного определения мутаций. Конечным результатом является анализ, в котором кровь непосредственно добавляется в реакционную пробирку для выявления мутаций, связанных с устойчивостью к противомалярийным лекарственным препаратам”, — говорит старший автор исследования доктор Фредерик Р. Хазелтон (Frederick R. Haselton), профессор биомедицинской инженерии и химии в Университете Вандербильта.
Исследование устойчивости к малярии было опубликовано в интернет-издании Journal of Molecular Diagnostics от 13 июня 2019 года.
Ссылки по теме:
Vanderbilt University
Latest Молекулярная диагностика News
Channels
Clinical Chemistry
view channel
3D Printed Point-Of-Care Mass Spectrometer Outperforms State-Of-The-Art Models
Mass spectrometry is a precise technique for identifying the chemical components of a sample and has significant potential for monitoring chronic illness health states, such as measuring hormone levels... Read more.jpg)
POC Biomedical Test Spins Water Droplet Using Sound Waves for Cancer Detection
Exosomes, tiny cellular bioparticles carrying a specific set of proteins, lipids, and genetic materials, play a crucial role in cell communication and hold promise for non-invasive diagnostics.... Read more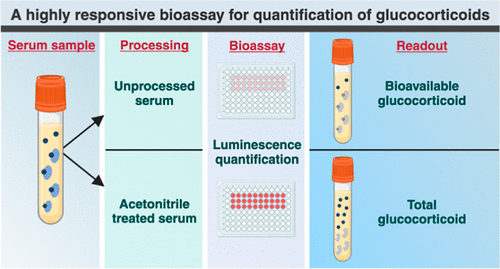
Highly Reliable Cell-Based Assay Enables Accurate Diagnosis of Endocrine Diseases
The conventional methods for measuring free cortisol, the body's stress hormone, from blood or saliva are quite demanding and require sample processing. The most common method, therefore, involves collecting... Read moreMolecular Diagnostics
view channel
Blood Test Predicts Knee Osteoarthritis Eight Years Before Signs Appears On X-Rays
Osteoarthritis (OA) is the most prevalent form of arthritis, impacting millions worldwide and resulting in significant economic and social costs. Although no cure exists currently, the effectiveness of... Read more
Blood Test Accurately Predicts Lung Cancer Risk and Reduces Need for Scans
Lung cancer is extremely hard to detect early due to the limitations of current screening technologies, which are costly, sometimes inaccurate, and less commonly endorsed by healthcare professionals compared... Read more
Unique Autoantibody Signature to Help Diagnose Multiple Sclerosis Years before Symptom Onset
Autoimmune diseases such as multiple sclerosis (MS) are thought to occur partly due to unusual immune responses to common infections. Early MS symptoms, including dizziness, spasms, and fatigue, often... Read more
Blood Test Could Detect HPV-Associated Cancers 10 Years before Clinical Diagnosis
Human papilloma virus (HPV) is known to cause various cancers, including those of the genitals, anus, mouth, throat, and cervix. HPV-associated oropharyngeal cancer (HPV+OPSCC) is the most common HPV-associated... Read moreHematology
view channel
Next Generation Instrument Screens for Hemoglobin Disorders in Newborns
Hemoglobinopathies, the most widespread inherited conditions globally, affect about 7% of the population as carriers, with 2.7% of newborns being born with these conditions. The spectrum of clinical manifestations... Read more
First 4-in-1 Nucleic Acid Test for Arbovirus Screening to Reduce Risk of Transfusion-Transmitted Infections
Arboviruses represent an emerging global health threat, exacerbated by climate change and increased international travel that is facilitating their spread across new regions. Chikungunya, dengue, West... Read more
POC Finger-Prick Blood Test Determines Risk of Neutropenic Sepsis in Patients Undergoing Chemotherapy
Neutropenia, a decrease in neutrophils (a type of white blood cell crucial for fighting infections), is a frequent side effect of certain cancer treatments. This condition elevates the risk of infections,... Read more
First Affordable and Rapid Test for Beta Thalassemia Demonstrates 99% Diagnostic Accuracy
Hemoglobin disorders rank as some of the most prevalent monogenic diseases globally. Among various hemoglobin disorders, beta thalassemia, a hereditary blood disorder, affects about 1.5% of the world's... Read moreImmunology
view channel
Diagnostic Blood Test for Cellular Rejection after Organ Transplant Could Replace Surgical Biopsies
Transplanted organs constantly face the risk of being rejected by the recipient's immune system which differentiates self from non-self using T cells and B cells. T cells are commonly associated with acute... Read more
AI Tool Precisely Matches Cancer Drugs to Patients Using Information from Each Tumor Cell
Current strategies for matching cancer patients with specific treatments often depend on bulk sequencing of tumor DNA and RNA, which provides an average profile from all cells within a tumor sample.... Read more
Genetic Testing Combined With Personalized Drug Screening On Tumor Samples to Revolutionize Cancer Treatment
Cancer treatment typically adheres to a standard of care—established, statistically validated regimens that are effective for the majority of patients. However, the disease’s inherent variability means... Read moreMicrobiology
view channel
New CE-Marked Hepatitis Assays to Help Diagnose Infections Earlier
According to the World Health Organization (WHO), an estimated 354 million individuals globally are afflicted with chronic hepatitis B or C. These viruses are the leading causes of liver cirrhosis, liver... Read more
1 Hour, Direct-From-Blood Multiplex PCR Test Identifies 95% of Sepsis-Causing Pathogens
Sepsis contributes to one in every three hospital deaths in the US, and globally, septic shock carries a mortality rate of 30-40%. Diagnosing sepsis early is challenging due to its non-specific symptoms... Read morePathology
view channel
First of Its Kind Universal Tool to Revolutionize Sample Collection for Diagnostic Tests
The COVID pandemic has dramatically reshaped the perception of diagnostics. Post the pandemic, a groundbreaking device that combines sample collection and processing into a single, easy-to-use disposable... Read moreAI-Powered Digital Imaging System to Revolutionize Cancer Diagnosis
The process of biopsy is important for confirming the presence of cancer. In the conventional histopathology technique, tissue is excised, sliced, stained, mounted on slides, and examined under a microscope... Read more
New Mycobacterium Tuberculosis Panel to Support Real-Time Surveillance and Combat Antimicrobial Resistance
Tuberculosis (TB), the leading cause of death from an infectious disease globally, is a contagious bacterial infection that primarily spreads through the coughing of patients with active pulmonary TB.... Read moreTechnology
view channel
New Diagnostic System Achieves PCR Testing Accuracy
While PCR tests are the gold standard of accuracy for virology testing, they come with limitations such as complexity, the need for skilled lab operators, and longer result times. They also require complex... Read more
DNA Biosensor Enables Early Diagnosis of Cervical Cancer
Molybdenum disulfide (MoS2), recognized for its potential to form two-dimensional nanosheets like graphene, is a material that's increasingly catching the eye of the scientific community.... Read more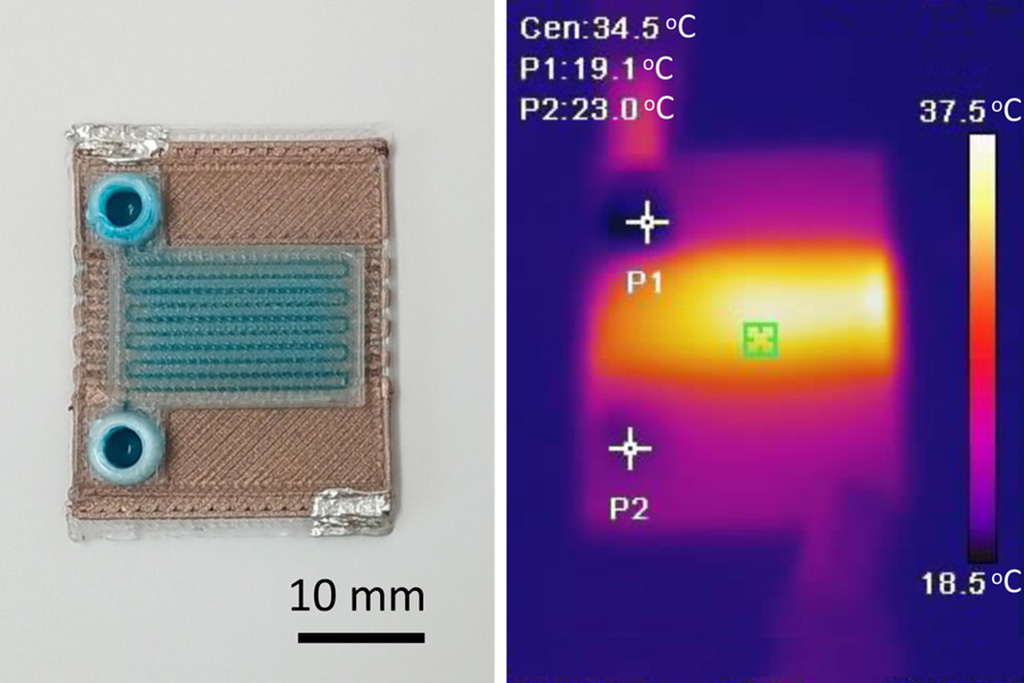
Self-Heating Microfluidic Devices Can Detect Diseases in Tiny Blood or Fluid Samples
Microfluidics, which are miniature devices that control the flow of liquids and facilitate chemical reactions, play a key role in disease detection from small samples of blood or other fluids.... Read more
Breakthrough in Diagnostic Technology Could Make On-The-Spot Testing Widely Accessible
Home testing gained significant importance during the COVID-19 pandemic, yet the availability of rapid tests is limited, and most of them can only drive one liquid across the strip, leading to continued... Read moreIndustry
view channel
ECCMID Congress Name Changes to ESCMID Global
Over the last few years, the European Society of Clinical Microbiology and Infectious Diseases (ESCMID, Basel, Switzerland) has evolved remarkably. The society is now stronger and broader than ever before... Read more
Bosch and Randox Partner to Make Strategic Investment in Vivalytic Analysis Platform
Given the presence of so many diseases, determining whether a patient is presenting the symptoms of a simple cold, the flu, or something as severe as life-threatening meningitis is usually only possible... Read more
Siemens to Close Fast Track Diagnostics Business
Siemens Healthineers (Erlangen, Germany) has announced its intention to close its Fast Track Diagnostics unit, a small collection of polymerase chain reaction (PCR) testing products that is part of the... Read more












.jpg)
