Обнаружена связь между кишечной флорой и рассеянным склерозом
|
By LabMedica International staff writers Posted on 26 Dec 2018 |
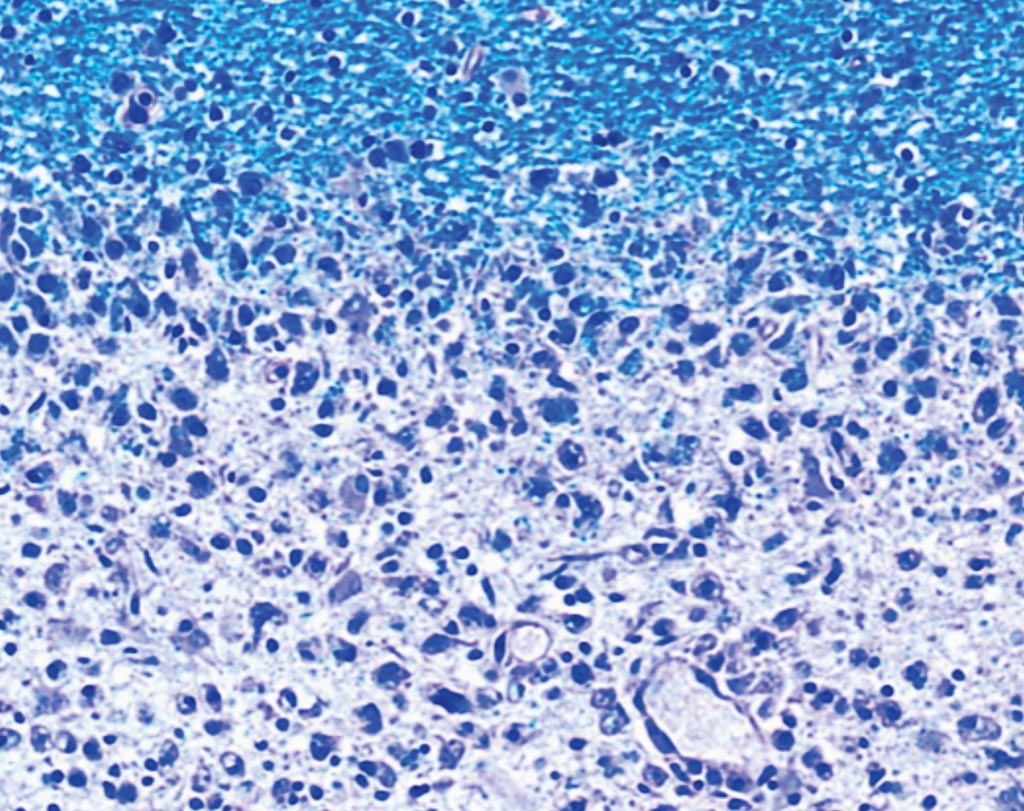
Уменьшение миелиновых оболочек: на поврежденных участках мозга пациентов (внизу изображения) с рассеянным склерозом не хватает миелина (вверху, синего цвета). Фото любезно предоставлено доктором медицины Имке Метц /Imke Metz/, Университет Геттингена.
Рассеянный склероз (РС) является иммуноопосредованным заболеванием центральной нервной системы, которое развивается у генетически восприимчивых людей и, по всей вероятности, требует триггеров со стороны окружающей среды. При РС собственная иммунная система организма атакует и повреждает защитное покрытие вокруг нервных клеток.
Аутоантигены и молекулярные имитаторы, активирующие аутоиммунный ответ при рассеянном склерозе, остаются не полностью понятыми. Хотя доподлинно установлено, что аутореактивные лимфоциты вызывают демиелинизацию при рассеянном склерозе, точные антигенные мишени, которые инициируют заболевание, не определены.
Международная группа ученых во главе с научными сотрудниками из Университетской клиники Цюриха (University Hospital Zurich; Цюрих, Швейцария) использовала инфильтрирующий клон CD4+ Т-клеток, который клонально размножается при поражениях мозга при рассеянном склерозе, и применила системный подход для идентификации его целевых антигенов, пептидные библиотеки в сочетании с биометрическим анализом. Для генетически определенной подгруппы пациентов с РС, обследованных учеными, результаты показывают, что кишечная микробиота может играть гораздо более важную роль в патогенезе заболевания, чем предполагалось ранее.
Команда определила гуанозиндифосфат(ГДФ)-L-фукозосинтазу (guanosine diphosphate (GDP)–l-fucose synthase) как аутоантиген, который распознается инфильтрирующими спинномозговой жидкостью CD4+ T-клетками от HLA-DRB3*-положительных пациентов. Были обнаружены значительные ассоциации между реактивностью к пептидам ГДФ-L-фукозосинтазы и экспрессией DRB3*02:02, а также реактивностью к иммунодоминантному пептиду основного белка миелина. Эти результаты, в сочетании с перекрестным распознаванием гомологичных пептидов из микробиоты кишечника, позволяют предположить возможную роль этого антигена в качестве индуктора или стимулятора патогенных аутоиммунных реакций при РС.
Клинический подход группы включает взятие крови у пациентов с РС в клинических испытаниях и прикрепление фрагментов иммуноактивного белка на поверхность эритроцитов в лаборатории. Когда кровь вновь вводится в кровоток пациентов, фрагменты помогают "перевоспитать" их иммунную систему и заставить ее "переносить" собственную мозговую ткань. Этот терапевтический подход направлен на эффективное целевое лечение без серьезных побочных эффектов.
Доктор медицины Мирея Соспедра Рамос (Mireia Sospedra Ramos), старший автор исследования, заявила: "Наш клинический подход специально нацелен на патологические аутореактивные иммунные клетки. Таким образом, этот подход радикально отличается от других методов лечения, доступных в настоящее время, которые блокируют всю иммунную систему. Хотя эти методы лечения часто помогают остановить прогрессирование заболевания, они также ослабляют иммунную систему и могут вызвать серьезные побочные эффекты". Исследование было опубликовано 10 октября 2018 года в журнале Science Translational Medicine.
Ссылки по теме:
Университетская клиника Цюриха
Аутоантигены и молекулярные имитаторы, активирующие аутоиммунный ответ при рассеянном склерозе, остаются не полностью понятыми. Хотя доподлинно установлено, что аутореактивные лимфоциты вызывают демиелинизацию при рассеянном склерозе, точные антигенные мишени, которые инициируют заболевание, не определены.
Международная группа ученых во главе с научными сотрудниками из Университетской клиники Цюриха (University Hospital Zurich; Цюрих, Швейцария) использовала инфильтрирующий клон CD4+ Т-клеток, который клонально размножается при поражениях мозга при рассеянном склерозе, и применила системный подход для идентификации его целевых антигенов, пептидные библиотеки в сочетании с биометрическим анализом. Для генетически определенной подгруппы пациентов с РС, обследованных учеными, результаты показывают, что кишечная микробиота может играть гораздо более важную роль в патогенезе заболевания, чем предполагалось ранее.
Команда определила гуанозиндифосфат(ГДФ)-L-фукозосинтазу (guanosine diphosphate (GDP)–l-fucose synthase) как аутоантиген, который распознается инфильтрирующими спинномозговой жидкостью CD4+ T-клетками от HLA-DRB3*-положительных пациентов. Были обнаружены значительные ассоциации между реактивностью к пептидам ГДФ-L-фукозосинтазы и экспрессией DRB3*02:02, а также реактивностью к иммунодоминантному пептиду основного белка миелина. Эти результаты, в сочетании с перекрестным распознаванием гомологичных пептидов из микробиоты кишечника, позволяют предположить возможную роль этого антигена в качестве индуктора или стимулятора патогенных аутоиммунных реакций при РС.
Клинический подход группы включает взятие крови у пациентов с РС в клинических испытаниях и прикрепление фрагментов иммуноактивного белка на поверхность эритроцитов в лаборатории. Когда кровь вновь вводится в кровоток пациентов, фрагменты помогают "перевоспитать" их иммунную систему и заставить ее "переносить" собственную мозговую ткань. Этот терапевтический подход направлен на эффективное целевое лечение без серьезных побочных эффектов.
Доктор медицины Мирея Соспедра Рамос (Mireia Sospedra Ramos), старший автор исследования, заявила: "Наш клинический подход специально нацелен на патологические аутореактивные иммунные клетки. Таким образом, этот подход радикально отличается от других методов лечения, доступных в настоящее время, которые блокируют всю иммунную систему. Хотя эти методы лечения часто помогают остановить прогрессирование заболевания, они также ослабляют иммунную систему и могут вызвать серьезные побочные эффекты". Исследование было опубликовано 10 октября 2018 года в журнале Science Translational Medicine.
Ссылки по теме:
Университетская клиника Цюриха
Latest Иммунология News
Channels
Clinical Chemistry
view channel
3D Printed Point-Of-Care Mass Spectrometer Outperforms State-Of-The-Art Models
Mass spectrometry is a precise technique for identifying the chemical components of a sample and has significant potential for monitoring chronic illness health states, such as measuring hormone levels... Read more.jpg)
POC Biomedical Test Spins Water Droplet Using Sound Waves for Cancer Detection
Exosomes, tiny cellular bioparticles carrying a specific set of proteins, lipids, and genetic materials, play a crucial role in cell communication and hold promise for non-invasive diagnostics.... Read more
Highly Reliable Cell-Based Assay Enables Accurate Diagnosis of Endocrine Diseases
The conventional methods for measuring free cortisol, the body's stress hormone, from blood or saliva are quite demanding and require sample processing. The most common method, therefore, involves collecting... Read moreMolecular Diagnostics
view channel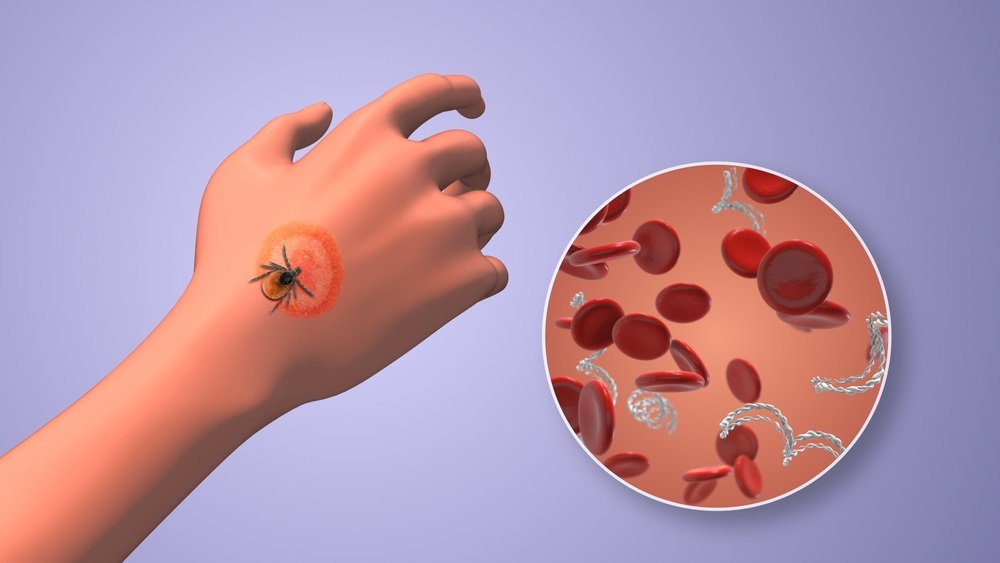
Urine Test to Revolutionize Lyme Disease Testing
Lyme disease is the most common animal-to-human transmitted disease in the United States, with around 476,000 people diagnosed and treated annually, and its incidence has been increasing.... Read more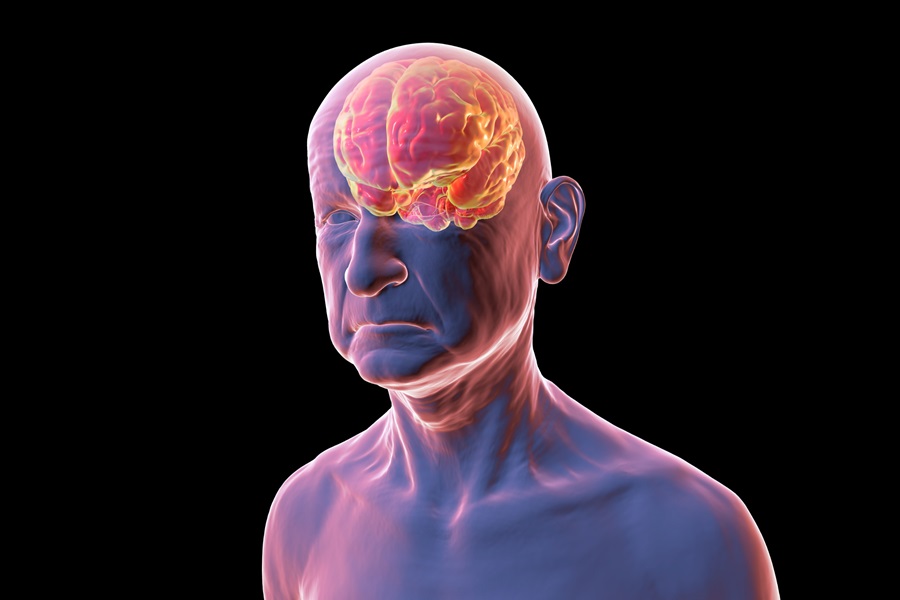
Simple Blood Test Could Enable First Quantitative Assessments for Future Cerebrovascular Disease
Cerebral small vessel disease is a common cause of stroke and cognitive decline, particularly in the elderly. Presently, assessing the risk for cerebral vascular diseases involves using a mix of diagnostic... Read more
New Genetic Testing Procedure Combined With Ultrasound Detects High Cardiovascular Risk
A key interest area in cardiovascular research today is the impact of clonal hematopoiesis on cardiovascular diseases. Clonal hematopoiesis results from mutations in hematopoietic stem cells and may lead... Read moreHematology
view channel
Next Generation Instrument Screens for Hemoglobin Disorders in Newborns
Hemoglobinopathies, the most widespread inherited conditions globally, affect about 7% of the population as carriers, with 2.7% of newborns being born with these conditions. The spectrum of clinical manifestations... Read more
First 4-in-1 Nucleic Acid Test for Arbovirus Screening to Reduce Risk of Transfusion-Transmitted Infections
Arboviruses represent an emerging global health threat, exacerbated by climate change and increased international travel that is facilitating their spread across new regions. Chikungunya, dengue, West... Read more
POC Finger-Prick Blood Test Determines Risk of Neutropenic Sepsis in Patients Undergoing Chemotherapy
Neutropenia, a decrease in neutrophils (a type of white blood cell crucial for fighting infections), is a frequent side effect of certain cancer treatments. This condition elevates the risk of infections,... Read more
First Affordable and Rapid Test for Beta Thalassemia Demonstrates 99% Diagnostic Accuracy
Hemoglobin disorders rank as some of the most prevalent monogenic diseases globally. Among various hemoglobin disorders, beta thalassemia, a hereditary blood disorder, affects about 1.5% of the world's... Read moreImmunology
view channel
Diagnostic Blood Test for Cellular Rejection after Organ Transplant Could Replace Surgical Biopsies
Transplanted organs constantly face the risk of being rejected by the recipient's immune system which differentiates self from non-self using T cells and B cells. T cells are commonly associated with acute... Read more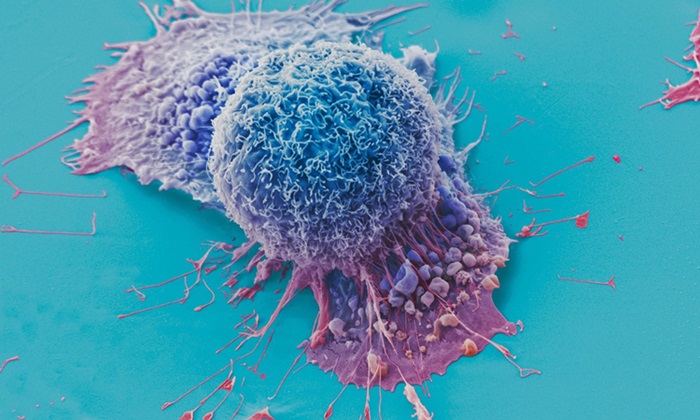
AI Tool Precisely Matches Cancer Drugs to Patients Using Information from Each Tumor Cell
Current strategies for matching cancer patients with specific treatments often depend on bulk sequencing of tumor DNA and RNA, which provides an average profile from all cells within a tumor sample.... Read more
Genetic Testing Combined With Personalized Drug Screening On Tumor Samples to Revolutionize Cancer Treatment
Cancer treatment typically adheres to a standard of care—established, statistically validated regimens that are effective for the majority of patients. However, the disease’s inherent variability means... Read moreMicrobiology
view channelEnhanced Rapid Syndromic Molecular Diagnostic Solution Detects Broad Range of Infectious Diseases
GenMark Diagnostics (Carlsbad, CA, USA), a member of the Roche Group (Basel, Switzerland), has rebranded its ePlex® system as the cobas eplex system. This rebranding under the globally renowned cobas name... Read more
Clinical Decision Support Software a Game-Changer in Antimicrobial Resistance Battle
Antimicrobial resistance (AMR) is a serious global public health concern that claims millions of lives every year. It primarily results from the inappropriate and excessive use of antibiotics, which reduces... Read more
New CE-Marked Hepatitis Assays to Help Diagnose Infections Earlier
According to the World Health Organization (WHO), an estimated 354 million individuals globally are afflicted with chronic hepatitis B or C. These viruses are the leading causes of liver cirrhosis, liver... Read more
1 Hour, Direct-From-Blood Multiplex PCR Test Identifies 95% of Sepsis-Causing Pathogens
Sepsis contributes to one in every three hospital deaths in the US, and globally, septic shock carries a mortality rate of 30-40%. Diagnosing sepsis early is challenging due to its non-specific symptoms... Read morePathology
view channel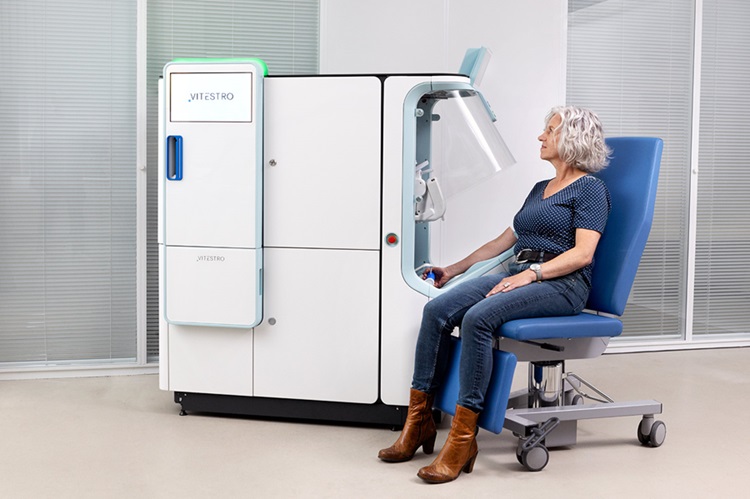
Robotic Blood Drawing Device to Revolutionize Sample Collection for Diagnostic Testing
Blood drawing is performed billions of times each year worldwide, playing a critical role in diagnostic procedures. Despite its importance, clinical laboratories are dealing with significant staff shortages,... Read more.jpg)
Use of DICOM Images for Pathology Diagnostics Marks Significant Step towards Standardization
Digital pathology is rapidly becoming a key aspect of modern healthcare, transforming the practice of pathology as laboratories worldwide adopt this advanced technology. Digital pathology systems allow... Read more
First of Its Kind Universal Tool to Revolutionize Sample Collection for Diagnostic Tests
The COVID pandemic has dramatically reshaped the perception of diagnostics. Post the pandemic, a groundbreaking device that combines sample collection and processing into a single, easy-to-use disposable... Read moreTechnology
view channel
New Diagnostic System Achieves PCR Testing Accuracy
While PCR tests are the gold standard of accuracy for virology testing, they come with limitations such as complexity, the need for skilled lab operators, and longer result times. They also require complex... Read more
DNA Biosensor Enables Early Diagnosis of Cervical Cancer
Molybdenum disulfide (MoS2), recognized for its potential to form two-dimensional nanosheets like graphene, is a material that's increasingly catching the eye of the scientific community.... Read more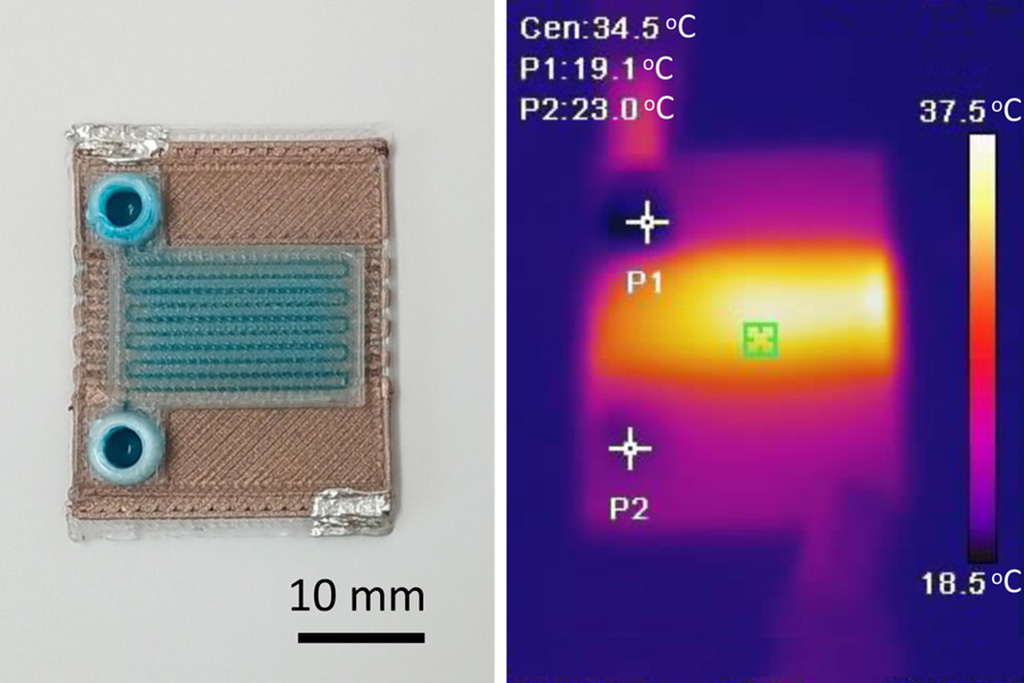
Self-Heating Microfluidic Devices Can Detect Diseases in Tiny Blood or Fluid Samples
Microfluidics, which are miniature devices that control the flow of liquids and facilitate chemical reactions, play a key role in disease detection from small samples of blood or other fluids.... Read more
Breakthrough in Diagnostic Technology Could Make On-The-Spot Testing Widely Accessible
Home testing gained significant importance during the COVID-19 pandemic, yet the availability of rapid tests is limited, and most of them can only drive one liquid across the strip, leading to continued... Read moreIndustry
view channel_1.jpg)
Thermo Fisher and Bio-Techne Enter Into Strategic Distribution Agreement for Europe
Thermo Fisher Scientific (Waltham, MA USA) has entered into a strategic distribution agreement with Bio-Techne Corporation (Minneapolis, MN, USA), resulting in a significant collaboration between two industry... Read more
ECCMID Congress Name Changes to ESCMID Global
Over the last few years, the European Society of Clinical Microbiology and Infectious Diseases (ESCMID, Basel, Switzerland) has evolved remarkably. The society is now stronger and broader than ever before... Read more